问题描述
人年纪大了,思维不灵活了,没以前那么快乐了,记忆力也变差了,感觉失去了活力,对喜怒哀乐各种情绪的体验变迟钝了。。。就连看海贼王也没有以前那么让我感动。。有没有逆转脑部衰老的方法?该怎么调整?我好怀念年轻时候的新鲜的情感和活力。怀念以前追海贼火影时候的热情还有快乐
脑部衰老的机制与逆转脑部衰老的方法
大家都知道,人年纪大了,记忆力就会下降了,这是为什么呢?有个涉及记忆的机制很重要——长时程增强作用,又称长期增益效应(Long-term potentiation,LTP),LTP是发生在两个神经元信号传输中的一种持久的增强现象,能够同步的刺激两个神经元。这是与突触可塑性——突触改变强度的能力相关的几种现象之一。由于记忆被认为是由突触强度的改变来编码的,LTP被普遍视为构成学习与记忆基础的主要分子机制之一。LTP随着年龄的增长而下降,原因包括(不限于)以下几种:
一、cAMP/CREB/BDNF信号改变可能导致了年龄相关的突触传递和 LTP 损伤。cAMP应答元件结合蛋白(cAMP response element binding protein,CREB)是一种转录增强因子,在神经元生成、突触可塑性及学习记忆等方面都具有重要的调节作用。CREB调控一种与大脑功能关系非常大的蛋白的表达——脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)。脑源性神经营养因子(BDNF)属于神经营养因子家族的重要成员,能够促进神经元的存活、分化、树突和轴突的生长,尤其在调节突触的可塑性中起关键作用,而神经元突触可塑性对神经环路的建立和控制脑的认知功能及复杂行为具有重要作用。BDNF对于神经元的功能维持非常重要,其一方面可以增加突触可塑性,进而影响长时程增强(long-term-ptentiati,LTP),一方面可以促进神经发生尤其是海马的神经发生,另一方面可以促进神经元的生存,特别是多巴胺与五羟色胺相关的神经元。这里发一张BDNF的通路图来说明BDNF是如何影响神经元功能的:
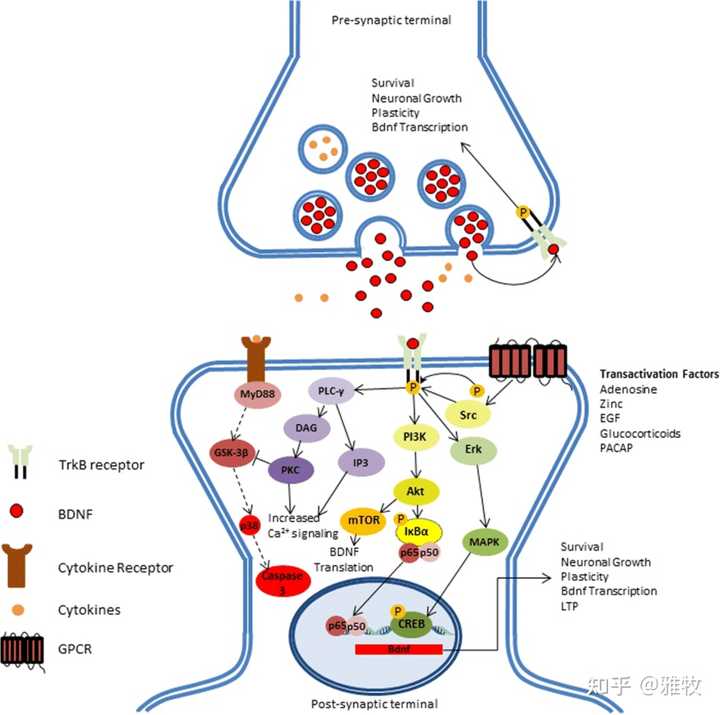
如图所示,BDNF-TrkB通路激活通过一系列细胞信号最终影响神经元的生存、生长、可塑性、BDNF转录与LTP。
这里发一张细胞通路图来说明cAMP是如何影响CREB表达的:
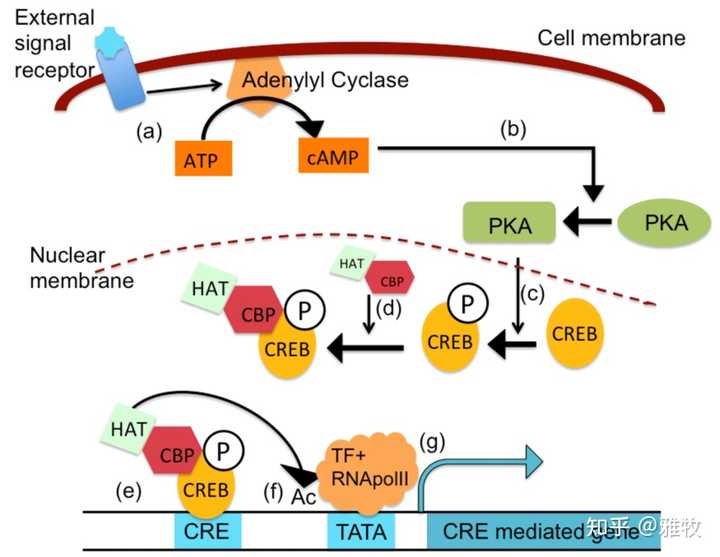
如图所示,当细胞中 cAMP 的水平升高时,cAMP 与 PKA 的调节亚基结合,使它们发生构象变化,释放活性催化亚基并使其底物磷酸化,而CRE 结合蛋白 (CREB1) 仅在被 PKA、MAPK 或 CaMK 磷酸化后才作为转录激活剂发挥作用。 Senescent-induced dysregulation of cAMP/CREB signaling and correlations with cognitive decline(衰老诱导的cAMP/CREB信号异常及其与认知功能下降的关系)这篇论文指出,随着衰老,cAMP/CREB信号发生变化,这与认知能力下降有关。而根据Alterations in the balance of protein kinase and phosphatase activities and age‐related impairments of synaptic transmission and long‐term potentiation(蛋白激酶和磷酸酶活性平衡的改变以及突触传递和长时程增强的年龄相关损伤)这篇论文,抑制cAMP损害LTP,而激活cAMP则可以恢复老年小鼠的LTP。
除了cAMP外,还有其他因素影响CREB的效应,这里再发一张图来说明诸多影响CREB的通路:
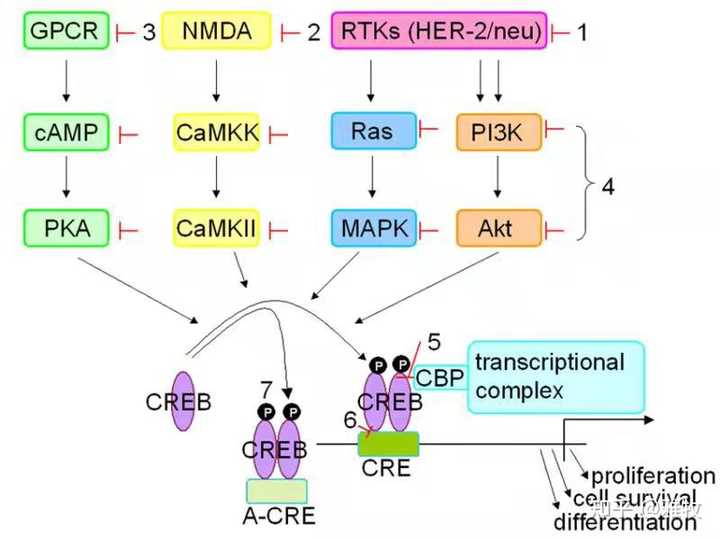
图片说明:环腺苷酸反应元件结合(CREB)蛋白具有多效性,在生理过程中,由于其在许多增长点下游的中心位置,信号通路CREB具有影响细胞存活、生长和发育的能力。从这个图里我们可以看到, NMDA也影响CREB的磷酸化,而知名促智药Noopept 正是一种 AMPA 和 NMDA的激活剂。
接下来再稍微详细谈下BDNF的作用。
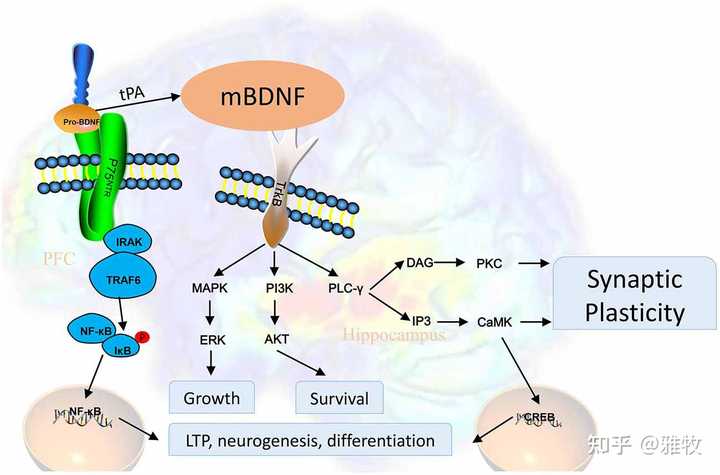
1、BDNF水平与衰老和认知能力的关系
在Higher brain BDNF gene expression is associated with slower cognitive decline in older adults(脑源性神经营养因子基因的高表达与老年人认知能力下降缓慢相关)这篇论文中,芝加哥拉什大学医学中心研究了535位老人的BDNF水平和认知能力的关系,研究人员对他们进行持续随访,直到他们死亡(随访时长平均为6年),并且在每年通过认知和记忆评估工具评估老年人的认知功能。老人死后,研究人员对他们进行尸体解剖,以检测他们的脑源性神经营养因子的编码基因水平。结果表明,大脑BDNF水平更高的参与者的认知功能衰退得更慢,如图所示:
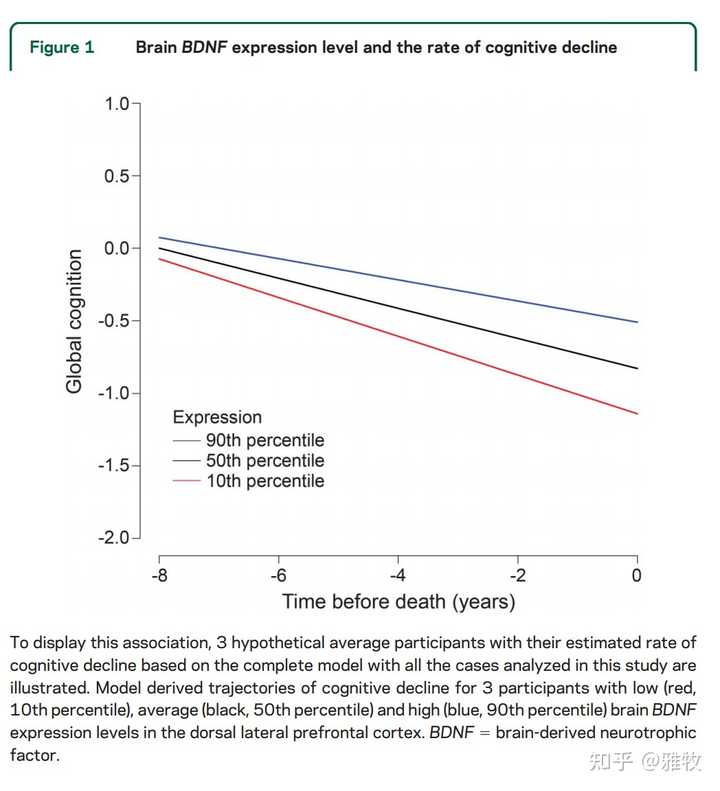
2、BDNF与压力、抑郁、自杀的关系
对临床前模型的研究表明,压力引起的 BDNF 表达失调。几种类型的压力源已被用于检查 BDNF 在压力相关疾病中的作用。外源性皮质酮的暴露(以模拟压力效应)也会降低啮齿动物海马体中 BDNF 的表达,类似于在各种临床前压力模型中观察到的情况。
BDNF 在抑郁症中的作用受到广泛关注,因为许多临床前和临床研究提供了直接证据,表明 BDNF 表达的调节可能与抑郁症相关的行为现象有关。此外,抑郁症患者在血细胞和死后脑组织中的 BDNF 表达均发生改变。遗传研究还将 BDNF 多态性与抑郁症联系起来。
Brain-derived Neurotrophic Factor: Role in Depression and Suicide(脑源性神经营养因子在抑郁症和自杀中的作用) 这篇论文研究检测了21 名完全表征的自杀受试者和 27 名非精神病健康对照受试者的标本,确定了 PFC(布罗德曼区 9)和海马中 BDNF 的 mRNA 和蛋白质表达。结果表明,与非精神病健康对照受试者相比,自杀受试者的 PFC 和海马体中 BDNF 的 mRNA 水平显着降低。
3、BDNF与睡眠的关系
根据Serum brain-derived neurotrophic factor (BDNF) in sleep-disordered patients: relation to sleep stage N3 and rapid eye movement (REM) sleep across diagnostic entities(睡眠障碍患者的血清脑源性神经营养因子(BDNF):与诊断实体的睡眠N3期和快速眼动(REM)睡眠的关系)这篇研究,低BDNF水平与 N3 期睡眠和快速眼动睡眠的低百分比相关。根据Sleep and aging: 1. Sleep disorders commonly found in older people(睡眠与衰老:1.老年人常见的睡眠障碍)这篇研究,老年人睡眠时的N3期和REM期减少,两个研究结合来看,我们可以合理推测:老年人睡眠质量降低可能跟BDNF水平下降有关。
4、BDNF基因
BDNF基因rs6265,是脑源性神经营养因子BDNF基因中的一个SNP(单核苷酸多态性),分为:
G 等位基因编码 Val(C)
A 等位基因编码 Met(T)。
每个等位基因都与不同水平的 BDNF 相关,“CC”产生最多的BDNF,“TT”产生最少,“CT”产生的BDNF则介于CC和TT之间。
研究显示,不同族群之间的BDNF基因型频率之间存在差异,60-65% 的白人人口具有“CC”基因型,而这种基因型出现在不到 30% 的中国人口中。与此相关的是,大约 90% 的黑人人口具有“CC”基因型——而一些非洲种族群体的“CC”基因型比例高达 98%(例如约鲁巴人)。
我们前面提到,BDNF与睡眠有关系,那么BDNF基因影响睡眠吗,根据The BDNF Val66Met Polymorphism Modulates Sleep Intensity: EEG Frequency- and State-Specificity这篇研究,拥有BDMF rs6265的“CC”(纯合)基因型的人,每晚大约多 20 分钟的“慢波”睡眠(第 3 阶段和第 4 阶段睡眠),同时“浅表”阶段(第 2 阶段睡眠)和整体“睡眠强度”增加(与“CT”相比) ,清醒时有更多的 alpha脑电波活动,以及REM(快速眼动期)睡眠期间有更多的alpha-、theta-和sigma脑电波活动(与“CT”相比)。
一些研究发现BDNF rs6265的基因型与认知能力有关,但另一些研究则显示无法找到强力证据。涉及认知能力的基因非常多,BDNF基因的影响还是很有限的。
更多关于BDNF基因的研究资料可参考:Potential Effects of rs6265 (BDNF): Stress, Weight, Cognition + More - SelfHacked
5、BDNF与性格的关系
研究发现,COMT和BDNF作为大脑中多巴胺可用性和释放的调节剂,已证明对人类认知的相互作用。根据BDNF Val66Met is Associated with Introversion and Interacts with 5-HTTLPR to Influence Neuroticism这篇研究,BDNF调节多种神经递质系统,包括血清素、多巴胺和谷氨酸,BDNF Val66Met 多态性 (rs6265) 与外向性相关。Met (T)携带者更内向。诸多研究显示,多巴胺水平随着年龄增长而下降,BDNF调节多巴胺,而年龄相关的cAMP/CREB/BDNF信号改变可能是随着年龄增长多巴胺水平下降的一个原因。
二、年龄增长带来的综合应激反应(ISR)可能导致了记忆力的损伤。ISR和eIF2B功能改变有关。eIF2B(eukaryotic initiation factor 2B,真核起始因子2B)是一种参与真核翻译起始的重要的蛋白质,也是一种鸟苷酸交换因子。eIF2B是一种多亚基复合物,包含五个亚基,分别为α、β、γ、δ和ε。综合应激反应(integrated stress response;ISR)是蛋白质稳态失调时诱发的信号中心调控网络,主要以控制蛋白质合成速率来实现,这种调控涉及eIF2三元复合物(ternary complex)的功能,eIF2三元复合物是一种异源三聚体,是由真核翻译起始因子eIF2(α、β和γ亚基组成)、GTP和带电荷甲硫酰基-起始转运RNA(Met-tRNAi)组成,eIF2三元复合物使eIF2B能够敏感地被磷酸化的eIF2的α亚基所抑制,从而调控真核生物的蛋白质翻译。这里发一张通路图来说明其如何影响记忆力和神经元状态:
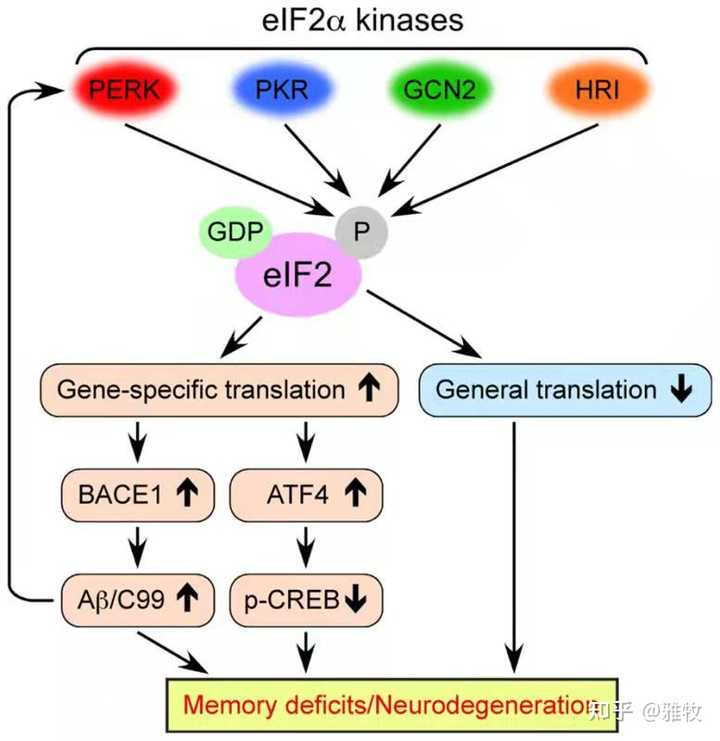
eIF2α是eLF2的α亚基,修饰eIF2α的蛋白酶就是eIF2α激酶,eIF2α的磷酸化不利于蛋白质翻译。目前发现了四种磷酸化eIF2α的丝氨酸琳氨酸蛋白激酶,分别是HRI,PERK,PKR及GCN2(如上图所示),这四种蛋白激酶通过磷酸化真核起始因子eIF2的α亚基来减弱mRNA翻译,这其中就包括磷酸化cAMP反应元件结合蛋白(p-CREB)水平的下降,而正如我们在上文种提到的那样,CREB和LTP关系很大。如图所示,eIF2α的磷酸化也会提升β-淀粉样蛋白(amyloid β-protein,Aβ),我们知道,具有神经毒性的Aβ的沉积是包括阿尔茨海默症(老年痴呆症)、帕金森症等神经退行性疾病的重要特征。
2020年12月份发布于Elife的论文“Small molecule cognitive enhancer reverses age-related memory decline in mice”中研究了一种叫ISRIB的化合物对于衰老小鼠的记忆力的影响,论文发现ISRIB可以逆转小鼠脑部衰老,而ISRIB正是一种ISR抑制剂,其是一种PERK抑制剂,通过抑制PERK可以调控elF2α磷酸化。小分子 ISRIB 通过抑制elF2α磷酸化从而激活eLF2B,起到拮抗综合应激反应 (ISR) 的激活作用。
PKR也是磷酸化eIF2α的四种激酶之一 ,抑制PKR也能改善记忆力吗?是的,目前已经有一些相关研究,比如说在PKR Inhibition Rescues Memory Deficit and ATF4 Overexpression in ApoE ε4 Human Replacement Mice(PKR抑制拯救ApoEε4人类替代小鼠的记忆缺陷和ATF4过度表达)这篇研究中,研究中通过给ApoE4小鼠注射PKR抑制剂,发现其可挽救记忆损伤并减弱ATF4在ApoE4小鼠中mRNA表达增加。在Suppression of PKR Promotes Network Excitability and Enhanced Cognition by Interferon-γ-Mediated Disinhibition(抑制PKR可通过干扰素-γ介导的去抑制促进网络兴奋性和增强认知能力)这篇研究中,作者探索了PKR和记忆力的关系,研究发现,PKR的缺失增加了海马脑片中长时程突触增强(L-LTP)。这些效应是由γ-干扰素(IFN-γ)介导的选择性减少GABA能突触作用引起的。总之,该研究结果表明,PKR可以很好地调节网络活动,而这些活动必须在学习过程中存储给定的片段。由于PKR活性在几种神经系统疾病中发生改变,这种激酶为治疗认知功能障碍提供了一个有希望的新靶点。作为这一方向的第一步,该研究证明选择性PKR抑制剂可以起到和PKR缺失小鼠类似的表现。
三、表观遗传与记忆力
我们知道,我们身上所有的细胞都是从受精卵分裂出来的,我们身上的所有细胞都拥有同一套DNA,但不同细胞拥有不同功能,这是由于每个细胞表达的基因和蛋白不同,而这导致不同细胞拥有不同的功能。表观遗传的改变主要表现为DNA序列不变而基因表达和细胞表型发生改变,这种表现是由表观遗传修饰导致的,表观遗传修饰包括组蛋白修饰和DNA甲基化等。我们在上文提到的CREB的相关的一种蛋白CREBPP(CREB结合蛋白)是一种与染色质修饰相关的蛋白(组蛋白乙酰化酶)。
随着衰老,细胞的表观遗传发生来改变,我们是否可以扭转这个过程?当然可以,这就需要用到重编程技术了,重编程(Reprogramming ) 是指在不改变基因序列的情况下,通过改变表观遗传修饰如DNA甲基化、乙酰化等来改变细胞命运的过程。大家都听说过克隆动物,克隆动物是怎么生产出来的?克隆动物的操作流程中包含一个步骤:将动物体细胞的细胞核移入去核卵母细胞中,在这个过程中,细胞核发生了重编程。2006年,日本京都大学山中伸弥在世界著名学术杂志《细胞》上率先报道了诱导多能干细胞的研究,他们把Oct3/4、Sox2、c-Myc和Klf4这四种转录因子(我们称之为“山中因子”)基因克隆入病毒载体,然后转染小鼠成纤维细胞,使小鼠成纤维细胞重编程,成为类似于胚胎干细胞的诱导性多能干细胞(induced pluripotent stem cells,iPS cells)。2012年,山中伸弥因此获得诺贝尔生理与医学奖。那么我们可以利用山中因子在动物身上实现返老还童吗?答案是可以,早在2016年,Salk研究所的研究人员就发现,通过对早衰小鼠进行短期的重编程处理可以将其寿命延长30%,相关论文:
In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming(通过部分重编程在体内改善与年龄相关的特征)
这篇论文里用了一个所谓的partial reprogramming(局部重编程)技术,这个技术通过循环短暂地诱导山中因子来实现局部重编程,为什么要循环短暂地诱导山中因子?因为持续不断地诱导山中因子表达,会使活体产生肿瘤。近来一篇发表于《Stem Cell Report》的论文用的也是这种方法:
In Vivo Reprogramming Ameliorates Aging Features in Dentate Gyrus Cells and Improves Memory in Mice(体内重编程可改善齿状回细胞的衰老特征并改善小鼠的记忆)
这篇论文发现,通过循环重编程技术可以逆转老年小鼠的认知能力。通过基因治疗来直接调控基因表达对于普通人来说还是比较遥远的(价格、安全性等都存在问题),而对我们来说通过使用小分子化合物来逆转脑部衰老更具有实用性。我这里再介绍几个表观遗传相关的通路是如何影响记忆力的:
1、Wnt信号通路
Wnt信号通路是一个复杂的蛋白质作用网络,参与胚胎发育、癌症、成年动物的正常生理过程。糖原合成酶激酶-3 (GSK-3)是Wnt信号通路的一个环节,糖原合成酶激酶-3 (GSK-3) 是一种在进化上非常保守的丝氨酸/苏氨酸激酶,普遍存在于哺乳动物真核细胞中,除去最早发现的调控糖原合成酶的活性外,GSK-3β还能作用于众多信号蛋白结构蛋白和转录因子,调节细胞的分化、增殖、存活和凋亡。Wnt信号通路与神经发育关系很大,我们先看一张信号通路图来看看Wnt信号通路是如何影响神经发育的:
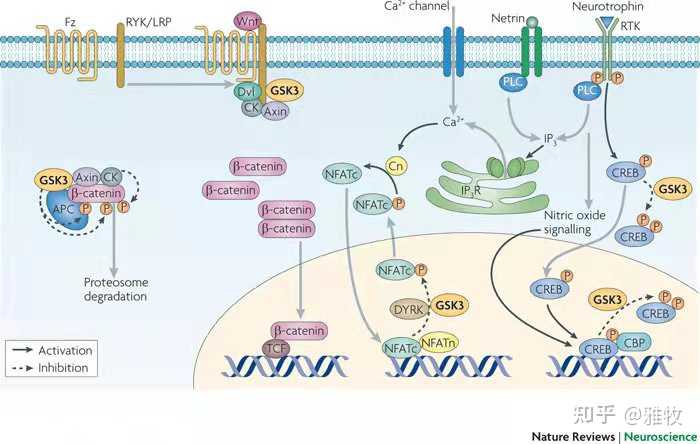
如图所示,GSK3可以磷酸化β-catenin ,β-catenin接着能够被APC复合物泛素化并降解,无法入核启动下游基因转录,也就是说,GSK3抑制了下游基因的转录,而抑制GSK3则可以增加下游基因的转录,此外GSK3还会下调CREB,从而影响神经元功能。
根据The GSK-3β/β-Catenin Signaling–Mediated Brain–Derived Neurotrophic Factor Pathway Is Involved in Aluminum-Induced Impairment of Hippocampal LTP In Vivo(活体中GSK-3β/β-连环蛋白信号介导的脑源性神经营养因子途径参与铝诱导的海马LTP损伤)这篇论文,GSK-3β 抑制剂SB216763上调了 BDNF 和 β-catenin 蛋白表达。在一项针对锂治疗对 AD(阿尔茨海默病) 患者的疗效的研究(Increase of BDNF serum concentration in lithium treated patients with early Alzheimer's disease;锂治疗早期阿尔茨海默病患者BDNF血清浓度升高)发现,与安慰剂治疗的患者相比,在接受锂治疗的 AD 患者中,BDNF 血清水平显著增加。锂盐中的碳酸锂被用于治疗狂躁症。
2、组蛋白修饰
组蛋白(histone)是真核生物体细胞染色质与原核细胞中的碱性蛋白质,和DNA共同组成核小体结构。它们是染色质的主要蛋白质组分,作为DNA缠绕的线轴,并在基因调控中发挥作用。组蛋白示意图:
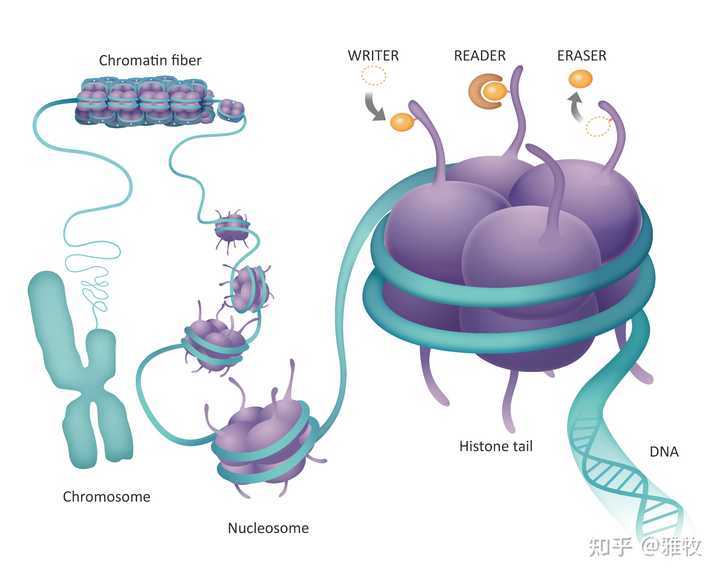
如图所示,DNA缠绕在组蛋白上形成核小体。核小体的核心颗粒再由DNA和组蛋白H1共同构成的连接区连接起来形成串珠状的染色质纤维,染色质纤维继续压缩,最终形成染色体。通过压缩,我们的DNA最终才能被塞进小小的细胞核。
组蛋白修饰(histone modification)是指组蛋白在相关酶作用下发生甲基化、乙酰化、磷酸化、腺苷酸化、泛素化、ADP核糖基化等修饰的过程。组蛋白修饰影响基因表达,组蛋白的乙酰化有助于基因表达。组蛋白去乙酰化酶抑制剂(histone deacetylase inhibitor,HDACI),简称HDACIs,是一类化合物,有干扰组蛋白去乙酰化酶的功能。通过干扰组蛋白去乙酰化酶的功能,HDACI具有影响表观遗传的作用。
研究发现,伏立诺他 (SAHA) 、丙戊酸、曲古抑菌素A(TSA)等HDACI可诱导BDNF mRNA的增加。值得一提的是,cAMP激活剂、组蛋白去乙酰化酶抑制剂、GSK-3β抑制剂经常被用于小分子重编程。目前,小分子化合物可以完全取代山中因子对体细胞进行重编程使其成为诱导多功能干细胞,近年来学术界(及生物黑客界)开始出现一些将小分子重编程用于活体逆转衰老的尝试,目前这个领域需要探索的是有效安全的给药组合、给药方式、给药剂量等。
综上所述,脑部衰老涉及许多细胞通路,如果想比较有效地逆转脑部衰老,就需要调控多条通路了。
这里顺便介绍几种有助于改善记忆力的常见补充剂:
虾青素:AMPK激活剂,拥有水油双溶特性,使其轻松跨越血液大脑屏障,通过减轻氧化应激、改善海马损伤和上调 BDNF 表达延缓脑部衰老。
苏糖酸镁:唯一可以通过血脑屏障的镁补剂。目前的研究表明,脑镁的升高可能是一种以区域特异性方式增强突触可塑性的新方法,从而在不增强或损害恐惧记忆形成的情况下增强消退效果。脑镁的升高增加了 NMDA 受体 (NMDARs) 信号传导、BDNF 表达、突触前点的密度和 PFC 中的突触可塑性。
下面有人说建议吃NAD+前体改善脑部衰老,吃NAD+前体有助于改善脑力吗?本人从2019年初接触NAD+前体,早年在知乎接触NAD+前体的很多人都认识我,本人的体验是NAD+前体对改善记忆力有一点用,但效果很有限,我现在在服用表观遗传药物和eIF2B激活剂(PERK抑制剂和PKR抑制剂),发现这套组合效果比NAD+前体+AMPK激活剂组合好很多。本人是一个不服命的人,作为脑力工作者,脑力的衰退让我心忧并且我想逆天改命,所以我才努力研究如何逆转脑部衰老。而我愿意积极尝试各种方法,可能跟我的大五人格中的开放性维度比较高有关系,而这可能和我拥有BDNF rs6265 CC和COMT rs4680 AG等能够提高我多巴胺功能的基因有关,而我喜欢在知乎和大家分享知识或许和我拥有OXTR rs53576 GG基因有关系(我从小就挺乐于助人和分享的)。欢迎同样不愿意屈服于衰老、想要逆天改命的小伙伴多和我交流沟通哈!
参考文献:
Hansen R T , Zhang H T . Senescent-induced dysregulation of cAMP/CREB signaling and correlations with cognitive decline[J]. Brain Research, 2013, 1516:93-109.
Steven A , Seliger B . Control of CREB expression in tumors: from molecular mechanisms and signal transduction pathways to therapeutic target[J]. Oncotarget, 2016, 7(23):35454-35465.
Hansen RT 3rd, Zhang HT. Senescent-induced dysregulation of cAMP/CREB signaling and correlations with cognitive decline. Brain Res. 2013 Jun 21;1516:93-109. doi: 10.1016/j.brainres.2013.04.033. Epub 2013 Apr 25. PMID: 23623816; PMCID: PMC3760033.
Hsu K S , Huang C C , Liang Y C , et al. Alterations in the balance of protein kinase and phosphatase activities and age‐related impairments of synaptic transmission and long‐term potentiation[J]. Hippocampus, 2002, 12(6):787-802.
Aron, S, Buchman, et al. Higher brain BDNF gene expression is associated with slower cognitive decline in older adults[J]. Neurology, 2016.
Dwivedi Y . Brain-derived neurotrophic factor: Role in depression and suicide[J]. Neuropsychiatric Disease and Treatment, 2009, 5(1):433-449.
Deuschle M , Schredl M , Wisch C , et al. Serum brain‐derived neurotrophic factor (BDNF) in sleep‐disordered patients: relation to sleep stage N3 and rapid eye movement (REM) sleep across diagnostic entities[J]. Journal of Sleep Research, 2017.
Terracciano A , Tanaka T , Sutin A R , et al. BDNF Val66Met is Associated with Introversion and Interacts with 5-HTTLPR to Influence Neuroticism[J]. Neuropsychopharmacology.
Costa-Mattioli M, Walter P. The integrated stress response: From mechanism to disease. Science. 2020 Apr 24;368(6489):eaat5314. doi: 10.1126/science.aat5314. PMID: 32327570.
Krukowski K, Nolan A, Frias ES, Boone M, Ureta G, Grue K, Paladini MS, Elizarraras E, Delgado L, Bernales S, Walter P, Rosi S. Small molecule cognitive enhancer reverses age-related memory decline in mice. Elife. 2020 Dec 1;9:e62048. doi: 10.7554/eLife.62048. PMID: 33258451; PMCID: PMC7721440.
Zhu P , Huang W , Kalikulov D , et al. Suppression of PKR promotes network excitability and enhanced cognition by interferon-γ-mediated disinhibition.[J]. Cell, 2011, 147(6):1384-1396.
Zhang H , Han Y , Zhang L , et al. The GSK-3β/β-Catenin Signaling–Mediated Brain–Derived Neurotrophic Factor Pathway Is Involved in Aluminum-Induced Impairment of Hippocampal LTP In Vivo[J]. Biological Trace Element Research, 2021.
Sartor G , Malvezzi A , Kumar A , et al. Enhancement of BDNF Expression and Memory by HDAC Inhibition Requires BET Bromodomain Reader Proteins[J]. The Journal of Neuroscience, 2018.
Hasan M R , Kim J H , Kim Y J , et al. Effect of HDAC Inhibitors on Neuroprotection and Neurite Outgrowth in Primary Rat Cortical Neurons Following Ischemic Insult[J]. Neurochemical Research, 2013, 38(9):1921-1934.
Gowda K M D , Kumari N S , Ullal H . Role of astaxanthin in the modulation of brain-derived neurotrophic factor and spatial learning behavior in perinatally undernourished Wistar rats[J]. Nutritional Neuroscience, 2020, 23(6):422-431.
Abumaria N , Yin B , Zhang L , et al. Effects of elevation of brain magnesium on fear conditioning, fear extinction, and synaptic plasticity in the infralimbic prefrontal cortex and lateral amygdala.[J]. Journal of Neuroscience, 2011, 31(42):14871-14881.
相关阅读:
